
Энтропия термодинамической системы.Работа в термодинамике.
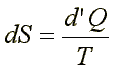
Основные понятия
- Энтропия – это мера вероятности пребывания системы в данном состоянии.
- Энтропия — мера рассеяния энергии. Это понятие также было введено Клаузиусом, который развил и облек второй принцип термодинамики в математическую форму: dS=d’Q/T. Энтропию стали называть «тенью» энергии. И энергия, и энтропия — слова греческого происхождения. «Эн» означает «способность» или «содержание», «эрг» — корень слова «работа», а «тропе» — «превращение», поэтому слово «энергия» можно перевести, как «способность совершения работы», а «энтропия» – как «способность к превращениям».
Законы, принципы и соотношения
dS=d’Q/T
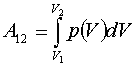
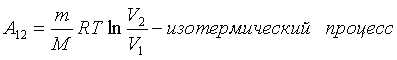
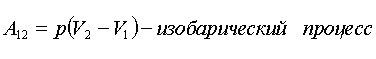
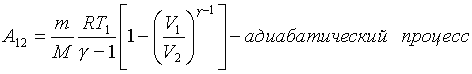
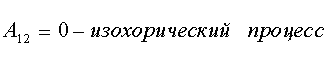
Энтропия термодинамической системы.
Энтропия — мера рассеяния энергии. Это понятие также было введено Клаузиусом, который развил и облек второй принцип термодинамики в математическую форму. Энтропию стали называть «тенью» энергии. И энергия, и энтропия — слова греческого происхождения. «Эн» означает «способность» или «содержание», «эрг» — корень слова «работа», а «тропе» — «превращение», поэтому слово «энергия» можно перевести, как «способность совершения работы», а «энтропия» – как «способность к превращениям».Энтропия зависит от характера совершающегося процесса, поскольку от него зависит как количество тепла, рассеивающееся вследствие прямого теплообмена системы с окружающей средой, так и количество тепла, выделяющееся и рассеивающееся вследствие трения. В действительности получаемая работа тоже зависит от характера процесса и никогда не бывает равна максимальной, то есть изменению энергии системы. Она меньше максимальной на величину потерь энергии «через тепло» из-за трения и теплообмена. Но и та часть энергии, которая расходуется на совершение работы, затем тоже вследствие трения и теплообмена рассеивается в окружающей среде, еще больше, повышая ее энтропию.
Так, вся энергия сгорающего бензина, превращающаяся в автомобильном двигателе в тепло, а затем в механическую энергию, в конечном итоге рассеивается в атмосфере в результате трения кузова о воздух и колес о воздух и землю.
Энтропия тела или системы может и уменьшаться. Например, когда мотор сообщает механическую энергию холодильнику, поглощающему тепло из морозильной камеры при температуре 00С и передающему его окружающему воздуху при 270С, энтропия морозильной камеры и всей системы уменьшится. Такое уменьшение не противоречит второму закону термодинамики, поскольку он применим лишь к замкнутым системам: при совместном рассмотрении всех частей системы полное изменение энтропии либо равно нулю, либо положительно.
Деятельность человека на Земле приводит к локальному уменьшению энтропии: холодильники и тепловые насосы способны перекачивать тепло от холодного тела к горячему. Всюду, где наблюдается локальное возрастание упорядоченности, противостоящее беспорядку, происходит локальное убывание энтропии. На Земле протекает естественный процесс концентрации энергии и уменьшения энтропии — процесс фотосинтеза, при котором рассеянная энергия солнечных лучей превращается в концентрированную химическую энергию зеленой массы растений.
В организмах же самых высокоупорядоченных на Земле систем — животных и человека — в процессе переваривания и усвоения пищи происходит дальнейшее уменьшение энтропии. Однако в целом наша Солнечная система, включающая в себя и первоисточник энергии - Солнце, характеризуется возрастанием суммарной энтропии. Исходя из этого факта, Клаузиус распространил закон возрастания энтропии в адиабатических системах не только на нашу Солнечную систему, но и на всю Вселенную, что привело его к выводу о грядущей тепловой смерти Вселенной, соответствующей достижению максимального значения её энтропии.
Через какой-то, пусть весьма длительный, промежуток времени, считал ученый, вся энергия, имеющаяся на Земле и в других частях Вселенной, превратится в тепло, а равномерное распределение последнего между всеми телами земной природы и Вселенной приведет к выравниванию температуры и полному прекращению каких бы то ни было превращений энергии — к «тепловой смерти Вселенной». «Можно оба главных положения механической теории теплоты, - писал он, - сформировать как основные законы Вселенной: энергия мира постоянна, энтропия мира стремиться к максимуму».
Но такое распространение второго закона термодинамики на всю Вселенную приводит к противоречию с принципом вечности движения во Вселенной, выражающимся в законе сохранения и превращения энергии.
В своих рассуждениях Клаузис исходил из допущения модели идеального газа, в котором молекулы движутся с одинаковой средней скоростью, что искажает реальную картину физических процессов.
Доказательство несостоятельности и критика теории тепловой смерти Вселенной были даны австрийским физиком Л. Больцманом: «Термодинамические понятия, полученные из изучения конечных систем на ограниченных интервалах времени, нельзя распространять на Вселенную, бесконечную во времени и пространстве».
Дальнейшее обобщение понятие энтропии получило в статистической физике. Согласно Л. Бопьцману, энтропия является мерой термодинамической вероятности W состояния системы. То есть при всяком взаимодействии реальных газов (диффузия, теплопроводность и т.д.) отдельные молекулы вступают во взаимодействие в согласии с законом теории вероятности. Энтропия связана с термодинамической вероятностью соотношением S = k ln W (k — постоянная Больцмана).
При этом под термодинамической вероятностью понимается число микросостояний системы (например, число различных состояний молекул в газе), посредством которых реализуется данное макросостояние. Условие термодинамического равновесия — максимальность энтропии, то есть термодинамическое равновесие имеет место в наиболее вероятном состоянии.
Больцман показал, что второе начало термодинамики не является абсолютным законом, а определяет лишь наиболее вероятное протекание процессов. Второе начало нарушается при флуктуациях в системе. Вместе с тем теряет абсолютный характер и термодинамическая необратимость, которая приобретает статистический смысл.
Термодинамическая необратимость, по Больцману, появляется только потому, что число микропроцессов, протекающих в одном направлении, подавляюще велико по сравнению с числом микропроцессов, протекающих в обратном направлении. Однако последняя вероятность не равна нулю; поэтому за достаточно большой промежуток времени в системе будет не только устанавливаться равновесное состояние, но и будут происходить любые отклонения от него. В макросистемах для этого требуются времена астрономического порядка. В микроскопических объёмах внутри окружающих нас тел такие изменения происходят всё время.
В отличие от закона сохранения энергии (всеобщего закона природы), второй закон термодинамики применим только к системам, состоящим из большого числа хаотически движущихся частиц и указываемое им направление протекания процессов является наиболее вероятным. Маловероятные противоположные процессы, называемые флуктуациями, не противоречат закону и также вытекают из него.
 |
 |
 |
 |
 |
 |