
Свойства энтропии. Объединенная формулировка I и II законов термодинамики: TdS>dU+pdV.
Основные понятия
- Энтропия — мера рассеяния энергии. Это понятие также было введено Клаузиусом, который развил и облек второй принцип термодинамики в математическую форму: dS=d’Q/T. Энтропию стали называть «тенью» энергии. И энергия, и энтропия — слова греческого происхождения. «Эн» означает «способность» или «содержание», «эрг» — корень слова «работа», а «тропе» — «превращение», поэтому слово «энергия» можно перевести, как «способность совершения работы», а «энтропия» – как «способность к превращениям».
Законы, принципы и соотношения
- Необратимый процесс (формулировка Клаузиуса) - процесс, при котором не происходит никаких изменений, кроме передачи тепла от горячего тела к холодному, является необратимым, иначе говоря, теплота не может спонтанно перейти от более холодного тела к более горячему без каких-либо других изменений в системе.
TdS>dU+pdV
Некоторые важнейшие свойства энтропии замкнутых систем
б) Энтропия замкнутой системы, совершающей необратимый цикл Карно, возрастает:
в) Энтропия замкнутой системы при любых, происходящих в ней процессах, не убывает: ΔS≥0.
При элементарном изменении состояния замкнутой системы энтропия не убывает: dS≥0.
Знак равенства относится к обратимым процессам, а знак неравенства к необ- ратимым. Пункт в) является одной из формулировок второго закона (начала) термодинамики.
Для произвольного процесса, происходящего в термодинамической системе, справедливо соотношение:
Свойства энтропии.
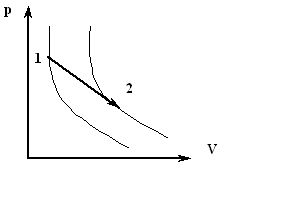
1. Итак, энтропия - функция состояния. Если процесс проводят вдоль адиабат, то энтропия системы не меняется. Значит адиабаты -это одновременно и изоэнтропы. Каждой более "высоко" расположенной адиабате (изоэнтропе) отвечает большее значение энтропии. В этом легко убедиться, проведя изотермический процесс между точками 1 и 2, лежащими на разных адиабатах (*см. рис.).
В этом процессе Т=const, поэтому S2-S1=Q/T. Для идеального газа Q равно работе А, совершаемой системой. А так как А>0, значит S2>S1.
Таким образом, зная, как выглядит система адиабат. Можно легко ответить на вопрос о приращении энтропии при проведении любого процесса между интересующими нас равновесными состояниями 1 и 2.
2. Энтропия- величина аддитивная: энтропия макросистемы равна сумме энтропий ее отдельных частей.
3. Одно из важнейших свойств энтропии заключается в том, что энтропия замкнутой (т.е. теплоизолированной) макросистемы не уменьшается - она либо возрастает, либо остается постоянной. Если же система не замкнута, то ее энтропия может как увеличиваться, так и уменьшаться.
Принцип возрастания энтропии замкнутых систем представляет собой еще одну формулировку второго начала термодинамики. Величина возрастания энтропии в замкнутой макросистеме может служить мерой необратимости процессов, протекающих в системе. В предельном случае, когда процессы имеют обратимый характер, энтропия замкнутой макросистемы не меняется.
Пример. Идеальный газ, находящийся в некотором состоянии, адиабатически (т.е. без теплообмена) расширили до объема V. Одинаково ли будет установившееся давление газа в конечном состоянии (в объеме V), если процесс расширения
а) обратимый,
б) необратимый?
В соответствии с принципом возрастания энтропии в замкнутой системе при необратимом процессе энтропия должна увеличиться. Значит установившееся состояние будет соответствовать точке на более высокой адиабате, т.е. давление будет больше.
Заметим, что с самого начала введение понятия энтропии S было поставлено в прямую связь с необратимостью. Оказывается, все самопроизвольно протекающие процессы в природе - от теплообмена до химических реакций - протекают так, что энтропия возрастает. Необходимо специальное взаимодействие с окружающей средой, что бы препятствовать возрастанию энтропии в макросистеме. Наиболее ярким примером могут служить все живые существа.
 |
 |
 |
 |
 |
 |